서 론
활성산소종(reactive oxygen species, ROS)은 인체의 대사과정에서 자연스럽게 생성되며 매우 불안정하고 반응성이 높아 DNA, 단백질, 지질 또는 탄수화물과 같은 생물학적으로 관련된 분자를 손상시키고(Fotina et al., 2013), 산화 스트레스를 유발시켜 알츠하이머병, 파킨슨병, 노화, 암 등 다양한 인간 질환을 초래한다(Dröge, 2002). 이러한 활성산소를 억제하는 항산화제는 다른 화학물질의 산화를 방지하는 화학물질로, 세포 대사의 자연 부산물인 유해한 활성산소의 영향을 중화하여 핵심 세포 구성요소를 보호한다(Badarinath et al., 2010). 현재 사용되고 있는 항산화제는 대부분 합성 항산화제로 비타민 C, 비타민 E, BHT(butylated hydroxytoluene), BHA(butylated hydroxyanisole) 등이 잘 알려져 있으며 천연 항산화제에 비해 항산화 활성이 높다는 장점이 있지만 장기 손상, 소화문제 등의 안전성 문제도 같이 제기되면서 천연물 유래 항산화 소재의 개발이 필요한 실정이다(Park and Cho, 2022; Zeng et al., 2011).
식용 곤충은 전통적인 식육 생산 방식인 가축에 비해 생산 주기가 짧아 공급이 용이한 식량 자원이며, 경제적 비용 절감과 및 항생제의 미사용, 온실가스 배출 절감을 통해 환경 오염을 감소시킬 수 있다는 장점이 있다(Zhou et al., 2022). 식용 곤충은 단백질 함량이 높고, 불포화 지방산, 미량 무기질 등의 영양소들이 풍부하게 함유되어 있으며, 특히 곤충 외부 표피층에 존재하는 지질체에서 합성된 다가 페놀층의 폴리페놀은 항산화, 항암, 항균 등의 다양한 생리적 활성을 나타내어 중요한 생물 자원으로 떠오르고 있다(Rice-Evans et al., 1997).
이러한 장점으로 식용곤충에 대한 활발한 연구가 진행되고 있는데, 항산화 활성 연구에서는 수벌번데기, 흰점박이꽃무지 유충, 누에나방 등이 사용되어 그 효과를 입증했으며(Anuduang et al., 2020; Ganguly et al., 2020; Kim et al., 2020). 항염증 연구에서는 장수풍뎅이, 메뚜기, 쌍별귀뚜라미 등이 활발히 연구되고 있다(Bahuguna et al., 2022; Lee et al., 2017a; Park et al., 2022). 또한 항암 연구도 진행되고 있는데, 쌍별귀뚜라미, 누에나방 등의 효과가 입증되고 있다(Kim et al., 2022; Suk et al., 2016).
이처럼 식품의약품안전처에서 인정한 10종의 식용곤충을 활용한 실험이 활발하게 진행되고 있고(Wedamulla et al., 2024), 갈색거저리 및 흰점박이꽃무지 유충을 활용한 항산화 활성 연구 또한 진행되고 있으나, 물 추출물을 이용한 항산화 활성의 연구는 미흡하다고 판단하였다. 따라서 본 연구는 갈색거저리 및 흰점박이꽃무지 유충을 활용하여 물 추출물을 제조해 항산화 활성을 확인하여 항산화제로써 사용방안을 제시하기 위해 수행하였으며, 이를 통해 식용곤충 유래 항산화제 개발에 도움을 주고자 하였다.
재료 및 방법
본 연구는 국내 식용곤충 농장에서 갈색거저리 유충(리프패럿, Busan, Korea) 및 흰점박이꽃무지 유충(굼벵이 브라더스, Incheon, Korea)을 구매하여 사용하였다. 2,2′-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid) diammonium salt, 2,2-Diphenyl-1-picrylhydrazyl(DPPH)시약은 Thermo Fisher Scientific (Seoul, Korea)에서 구입하여 사용하였다. Trichloroacetic acid, ferric chloride, sodium nitrite는 대정화금(Siheung, Korea)에서 구입해 사용하였다. Methanol, n-hexane은 Samchun(Seoul, Korea)에서 구입해 사용하였다. Phosphoric acid는 Yakuri Pure Chemicals(Kyoto, Japan)에서 구입하여 사용하였다. 10X dulbecco’s phosphate-buffered saline(10X DPBS), 10X trypsin-EDTA solution은 Welgene(Gyeongsan, Korea)에서 구입하여 사용하였다. Dulbecco’s modified Eagle’s medium (DMEM)은 Cytiva/Hyclone(Incheon, Korea)에서 구입하여 사용하였다. Cell counting kit-8(CCK-8)은 Do Gen bio(Seoul, Korea)에서 구입하여 사용하였다. Cell scraper, cell culture dish는 SPL life science(Pocheon, Korea)에서 구입하여 사용하였다. Sodium phosphate monobasic, sodium phosphate dibasic, sodium phosphate, potassium ferricyanide, sulfanilamide, naphthyl ethylenediamine dihydrochloride, L-Ascorbic acid, fetal bovine serum(FBS), penicillin/streptomycin(P/S), filter paper(Grade 2)는 Sigma-Aldrich (St. Louis, MO, USA)에서, 실험용 체(Φ230(w/Handle 265)× h90 mm)는 Daihan Scientific(Wonju, Korea)에서 구입하여 사용하였다. Shaking incubator는 DAIHAN LabTech (Namyangju, Korea)에서, CO2 incubator는 Panasonic(Osaka, Japan)에서, 원심분리기는 Hanil(Gimpo, Korea)에서, 교반기는 고려에이스과학(Seoul, Korea)에서 구입하여 사용하였다.
갈색거저리 및 흰점박이꽃무지의 유충을 각각 믹서기로 분쇄한 후 실험용 체를 이용하여 동일한 크기로 걸러주었다. 이후 곤충분말과 n-hexane을 1:3(w/v) 비율로 섞어 12시간동안 교반기를 이용하여 상온에서 600 rpm으로 진탕 후, 상층액을 제거하였으며 침전물의 잔여 n-hexane을 제거하기 위해 후드에서 6시간 이상 건조하였다. 각각의 최종 탈지분은 동결건조 후 –20℃ 동결고에 보관하며 사용하였다.
갈색거저리 및 흰점박이꽃무지 유충 탈지분말과 증류수를 1:10(w:v) 비율로 혼합한 뒤 shaking incubator를 사용하여 60℃에서 2시간동안 추출하였다. 이후 추출액은 filter paper를 이용하여 추출액을 여과하여 실험에 사용하였다.
RAW 264.7 cell은 한국세포주은행(Seoul, Korea)에서 분양 받아 사용하였다. 10% FBS와 1% P/S를 DMEM에 첨가하여 세포배양배지로 사용했으며, 세포는 37℃, 5% CO2 incubator에서 배양하였다.
RAW 264.7 cell을 96well plate에 5×104 cell/well의 농도로 분주한 후 incubator(37℃, 5% CO2)에서 24시간동안 배양한 뒤 양성 대조군(positive control, PC)에는 DMEM만, PC를 제외한 처리군에는 갈색거저리 및 흰점박이꽃무지 유충 물 추출물을 10, 20, 30, 40 및 50 mg/mL 농도로 처리하여 24시간동안 반응시켰다. PC를 제외한 처리군에 최종농도가 100 mM이 되도록 H2O2를 처리하고 incubator(37℃, 5% CO2)에서 4시간동안 반응시켰다. 이후 반응한 상층액을 모두 제거한 뒤, well에 DMEM과 혼합한 CCK-8 용액을 넣고 incubator(37℃, 5% CO2)에서 3시간 반응시킨 후 ELISA reader(INNO-S, Bio Mart, Daejeon, Republic of Korea)를 사용하여 450 nm에서 흡광도를 측정하였다.
7 mM ABTS 시약 및 2.5 mM potassium persulfate를 같은 비율로 희석한 뒤 0.01 M phosphate buffer(pH 7.4)를 혼합하여 734 nm에서 흡광도 값이 0.70±0.02으로 조정된 ABTS 용액을 제조 후 사용하였다. 갈색거저리 및 흰점박이꽃무지 유충 물 추출물을 농도별로 20 μL씩 처리한 뒤, 제조된 ABTS 용액 180 μL를 혼합하여 실온의 암실에서 10분간 반응시키고, ELISA reader(INNO-S, Bio Mart)를 사용하여 734 nm에서 흡광도를 측정하였으며 아래의 식으로 라디칼 소거활성을 계산하였다.
위 식의 A는 시료 무첨가 시 흡광도 값, B는 시료 첨가시 흡광도 값을 나타낸다.
MeOH를 사용하여 0.2 mM DPPH solution을 제조하였다. 갈색거저리 및 흰점박이꽃무지 유충 물 추출물을 e-tube에 농도별로 100 μL씩 처리한 뒤 DPPH solution을 300 μL처리하고 실온의 암실에서 30분 반응시켰다. 이후 원심분리기(Hanil)를 사용하여 침전물을 제외한 상층액을 96 well plate에 도포하여 517 nm에서 ELISA reader(INNO-S, Bio Mart)를 사용하여 흡광도를 측정하였으며 다음과 같이 라디칼 소거활성을 계산하였다.
위 식의 A는 시료 무첨가 시 흡광도 값, B는 시료 첨가시 흡광도 값을 나타낸다.
갈색거저리 및 흰점박이꽃무지 유충 물 추출물을 농도별로 100 μL씩 e-tube에 도포한 뒤 0.2 M phosphate buffer와 Potassium ferricyanide를 각각 100 μL씩 처리하고 50℃의 암실에서 20분간 반응시켰다. 이후 100 μL의 trichloroacetic acid를 처리한 뒤 600×g에서 5분간 원심분리하여 얻어진 100 μL의 상층액 및 증류수를 각각 넣고, 20 μL의 ferric chloride를 처리하여 700 nm에서 ELISA reader를 사용하여 흡광도를 측정하였다.
결과 및 고찰
H2O2와 같은 활성산소는 산화 스트레스를 유발하는 대표적인 물질로(Ha et al., 2015), RAW 264.7의 세포생존률을 측정하기 위해 산화스트레스제로 사용하였다. H2O2의 최적 농도는 가장 낮은 세포 생존률을 보인 100 mM로 선택하였으며, 100 mM H2O2의 처리는 세포 생존률을 PC 대비 40%까지 낮추어(p<0.05) 세포 독성을 확인하였다. RAW 264.7 세포에 적용되는 갈색거저리 및 흰점박이꽃무지 유충 물 추출물의 최종농도는 각각 10, 20, 30, 40, 50 mg/mL이며, 갈색거저리 및 흰점박이꽃무지 유충 물 추출물을 처리하였을 때의 세포활성도를 측정한 결과, 갈색거저리 및 흰점박이꽃무지 유충 물 추출물 모두 세포활성 저하를 억제시켜 세포를 산화스트레스 발생으로부터 보호해주는 것으로 판단된다(Fig. 1). 또한, 갈색거저리 유충 물 추출물은 PC군과 비교하였을 때 75.24% 수준의 세포생존율을 보였으며, 흰점박이꽃무지 유충 물 추출물이 처리된 세포의 활성보다 높은 세포생존율을 나타냈다. Baek 등(2017)은 갈색거저리 유충, 흰점박이꽃무지 유충 밎 장수풍뎅이 유충의 일반성분과 아미노산 및 지방산 조성 분석에서 갈색거저리 유충 및 흰점박이꽃무지 유충을 비교하였을 때 갈색거저리 유충에서 류신, 라이신, 발린 등의 필수 아미노산 함량이 흰점박이꽃무지 유충보다 높은 것을 확인하였다. 이중 류신과 발린은 BCAA(Branched-chain Amino Acids, 분지아미노산)에 속해 단백질 합성을 촉진하고 세포대사와 성장에 중요한 역할을 하며, 특히 류신은 세포성장, 생존, 대사를 조절하는 신호 전달 경로인 mTOR 경로를 활성화하여 세포성장과 생존에 긍정적인 영향을 미칠 수 있는 것으로 알려져있다(Kang et al., 2024). 따라서 갈색거저리 유충 내의 필수 아미노산이 세포활성 증가에 영향을 미쳐 갈색거저리 유충 물 추출물이 흰점박이꽃무지 유충 물 추출물보다 세포활성도가 높았을 가능성을 제시한다. 이로써 갈색거저리 및 흰점박이꽃무지 유충은 산화스트레스로부터 RAW 264.7 cell을 보호할 수 있는 것으로 사료된다.
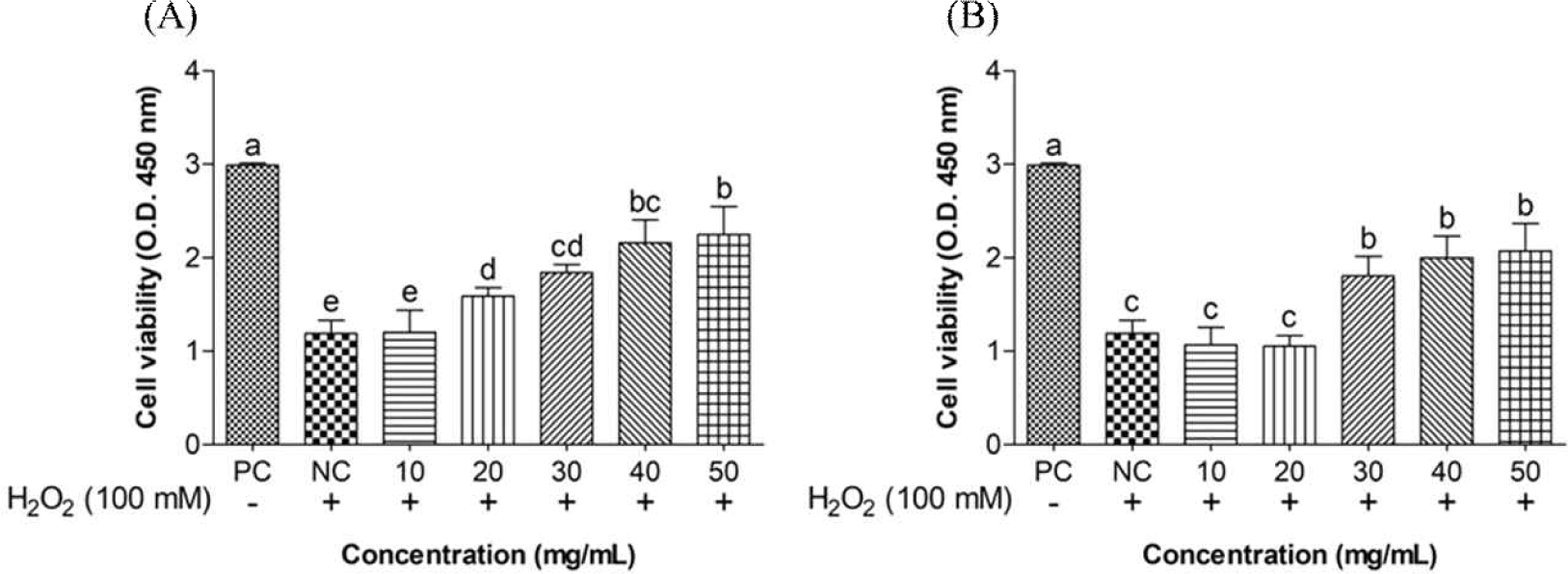
일반적으로 항산화 활성은 페놀 화합물의 함량과 양의 상관관계가 있으며(Fraga et al., 2019), 갈색거저리 및 흰점박이꽃무지 유충은 페놀화합물이 함유되어있다고 알려진 바 있다(Choi et al., 2023). 본 실험은 갈색거저리 및 흰점박이꽃무지 유충의 항산화 능력을 확인하기 위해 2, 4, 6, 8 및 10 mg/mL 농도로 물 추출물을 제조하여 ABTS, DPPH 라디칼 소거 활성 및 환원력을 측정하였다. ABTS 라디칼 소거 활성 측정법은 항산화 활성을 측정하는 대표적인 방법으로, ABTS와 과황산칼륨의 반응을 통해 청록색의 ABTS 라디칼 양이온이 생성되면 라디칼을 항산화제가 소거하여 ABTS가 탈색되는 원리를 따른다(Re et al., 1999). 갈색거저리 및 흰점박이꽃무지 유충 물 추출물의 ABTS 라디칼 소거능은 각각 농도가 증가함에 따라 32.12–59.60%, 39.59–79.08%까지 유의적으로 증가하였으며 모든 농도에서 갈색거저리 유충 물 추출물보다 흰점박이꽃무지 유충 물 추출물이 더 우수한 ABTS 라디칼 소거능을 보였다(Fig. 2). Yoon 등(2024)의 연구에 따르면 갈색거저리 유충 분말 함량을 달리하여 제조한 두유에서 갈색거저리 분말의 첨가량에 따라 ABTS 라디칼 소거능이 TML0(soymilk with 0% tenebrio)에 비해 39.03–77.75%까지 농도 의존적으로 증가하여 갈색거저리 유충 분말의 함량이 증가할수록 항산화 활성이 향상되는 것을 확인하였다. Lee 등(2021)의 갈색거저리 분말의 첨가량을 달리하여 제조한 양갱의 항산화 활성 측정 연구에서 갈색거저리 분말 함량이 증가함에 따라 ABTS 라디칼 소거능은 용량의존적으로 63.22–81.56%까지 유의하게 증가하는 것을 확인하였다. Lee 등(2017b)은 흰점박이꽃무지 유충 단백 가수분해물을 제조하여 항산화 활성을 평가한 결과 우수한 ABTS 라디칼 소거능을 확인하였다.
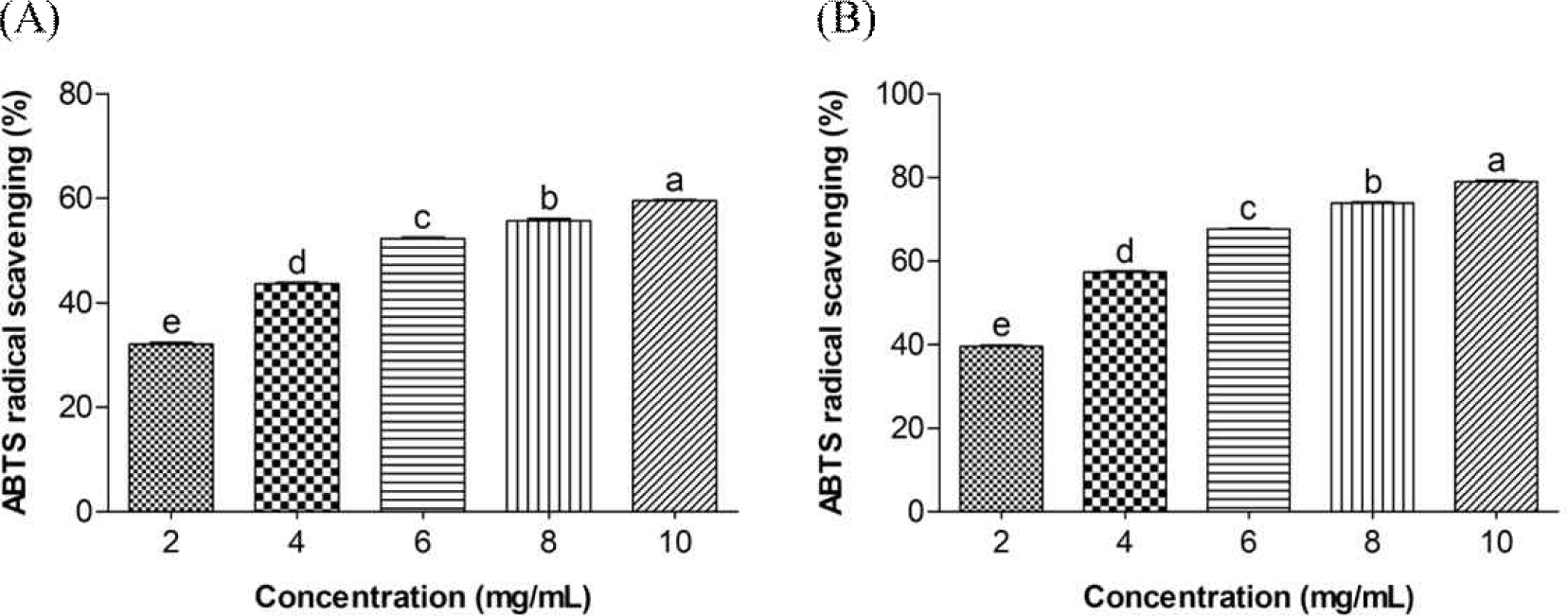
DPPH 라디칼 소거 활성 측정은 2,2-Diphenyl-1-picrylhydrazyl라는 안정된 자유라디칼을 이용하여 항산화를 측정하는 방법으로, 항산화제가 DPPH와 반응하게 되면 수소원자나 전자를 DPPH 라디칼에 공여하여 라디칼을 중성 분화로 환원시켜 DPPH 라디칼의 전자 구조를 변형시키는데, 이때 보라색에서 노란 계열의 옅은 색으로 색이 변하는 원리를 따른다(Marinova and Batchvarov, 2011). 이와 같은 원리로 갈색거저리 유충 및 흰점박이꽃무지 유충 물 추출물의 DPPH 라디칼 소거능을 측정한 결과, 두 물 추출물 모두 농도가 증가함에 따라 유의적으로 라디칼 소거 활성이 향상되었으며 모든 농도에서 갈색거저리 유충 물 추출물보다 흰점박이꽃무지 유충 물 추출물이 더 효과적으로 DPPH 라디칼을 소거하였다(Fig. 3). Ganguly 등(2020)은 흰점박이꽃무지에서 유래한 단백질 추출물의 항산화능을 평가하기 위해 DPPH 라디칼 소거능을 평가한 결과, 농도 의존적으로 효과적인 향상된 DPPH 라디칼 소거능을 확인하였다. Kim(2020)은 갈색거저리 유충 유래 오일(TMO)의 DPPH 라디칼 소거능을 평가하였는데, 그 결과 0.01, 0.05, 0.1 및 0.2%의 TMO는 각각 4.77, 17.04, 25.06 및 36.87% 수준으로 농도의존적으로 증가하였으며, 유의적인 DPPH 라디칼 소거능을 확인하였다. Chong 등(2017)은 갈색거저리 분말이 0, 10, 20 및 30% 함유된 쿠키를 제조하여 항산화 활성을 평가한 결과 아무것도 첨가하지 않은 쿠키와 비교했을 때 갈색거저리 분말의 첨가량이 증가할수록 항산화 활성은 증가하여 30% 첨가군에서 가장 높은 항산화 활성이 나타나는 것을 확인하였다.
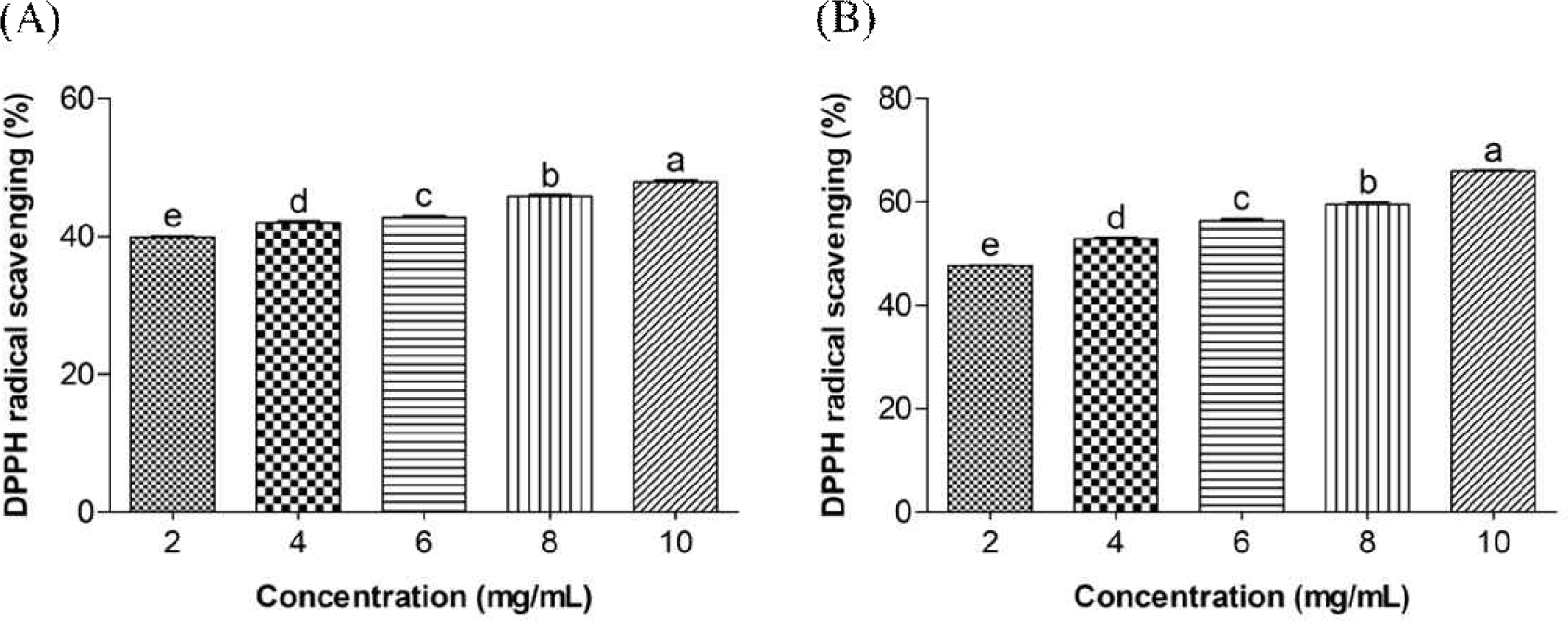
환원력은 산화제인 Potassium Ferricyanide가 항산화능을 가진 물질과 반응하면 Ferrocyanide로 환원되는 원리를 이용한 실험이다(Estabrook, 1961). 갈색거저리 유충 및 흰점박이꽃무지 유충 물 추출물에서 전체적인 환원력은 흰점박이꽃무지 유충 물 추출물에서 더 높게 나타났으며, 두 물 추출물 모두 농도 의존적으로 유의적인 환원력을 나타냈다(Fig. 4). Kim 등(2024)의 연구에서 온도별 흰점박이꽃무지 유충 물 추출물의 환원력을 알아보기 위해 75, 25, 5℃에서 각각 추출한 추출물의 환원력을 측정한 결과, 모든 온도에서 농도 의존적으로 환원력이 증가하였다. Park 등(2022)은 흰점박이꽃무지 유충 추출물과 발효흰점박이꽃무지 유충 추출물의 환원력을 비교한 결과, 흰점박이꽃무지 유충 추출물 및 발효흰점박이꽃무지 유충 추출물의 환원력은 농도의존적으로 증가하는 경향을 나타내어 흰점박이꽃무지 유충의 항산화능을 확인하였다. 그러므로, 갈색거저리 및 흰점박이꽃무지 유충 물 추출물은 우수한 항산화 소재로서 가능성이 있으며, 추가연구를 통해 항산화 효능을 가진 유효성분을 분석할 필요가 있다고 사료된다.

결 론
본 연구는 갈색거저리 및 흰점박이꽃무지 유충 물 추출물의 항산화 활성을 평가하기 위해 수행되었다. 갈색거저리 및 흰점박이꽃무지 유충은 H2O2처리된 RAW 264.7 cell에서 농도의존적으로 높은 세포활성을 보였으며, 갈색거저리 유충 물 추출물에서 더 우수한 세포 활성을 나타냈다. 갈색거저리 및 흰점박이꽃무지 유충은 모두 우수한 ABTS 및 DPPH 라디칼 소거능 및 환원력을 나타내 항산화 소재로서의 가능성을 확인하였다. 그러므로, 갈색거저리 및 흰점박이꽃무지는 우수한 항산화제로서 활용이 가능하며, 분리 정제 과정을 통해 이들의 항산화를 나타내는 유효성분 분석이 필요할 것이라 사료된다. 더 나아가 추가적인 생리활성 효능 검증 통해 다양한 기능성 식품소재로서의 가능성이 있음을 시사한다.
